a. Khái niệm
Hình 10.1. Một số hợp chất hữu cơ trong tự nhiên
Hợp chất hữu cơ là hợp chất của carbon (trừ một số các hợp chất vô cơ như carbon monoxide, carbon dioxide, muối carbonate, cyanide, carbide,...).
- Các hợp chất của carbon với các nguyên tố khác trong bảng tuần hoàn đã tạo nên hàng chục triệu hợp chất hữu cơ. Số lượng các chất hữu cơ mới vẫn đang tiếp tục tăng lên.
- Hoá học hữu cơ là ngành hoá học chuyên nghiên cứu các hợp chất hữu cơ.
b. Đặc điểm chung của các hợp chất hữu cơ
Thành phần phân tử nhất thiết phải chứa nguyên tố carbon, thường có hydrogen, oxygen, nitrogen, halogen, sulfur, phosphorus,...
- Liên kết hoá học chủ yếu là liên kết cộng hoá trị. Các nguyên tử carbon không những có khả năng liên kết với nguyên tử của các nguyên tố khác mà còn có thể liên kết với nhau tạo thành mạch carbon.
- Nhiệt độ nóng chảy thấp, nhiệt độ sôi thấp (dễ bay hơi) và thường không tan hoặc ít tan trong nước, tan trong các dung môi hữu cơ.
- Dễ cháy, kém bền với nhiệt nên dễ bị nhiệt phân huỷ.
- Phản ứng của các hợp chất hữu cơ thường xảy ra chậm, theo nhiều hướng và tạo ra hỗn hợp các sản phẩm. Để tăng tốc độ phản ứng thường cần đun nóng và có xúc tác.
1.2. Phân loại hợp chất hữu cơ
- Dựa vào thành phần nguyên tố, hợp chất hữu cơ có thể phân thành hai loại:
Hydrocarbon và dẫn xuất của hydrocarbon.
- Hydrocarbon là những hợp chất được tạo thành chỉ từ hai nguyên tố carbon và hydrogen. Một số hydrocarbon tiêu biểu:
- Khi một hay nhiều nguyên tử hydrogen trong phân tử hydrocarbon được thay thế bằng một hay nhiều nguyên tử hay nhóm nguyên tử khác (thường chứa oxygen, nitrogen, sulfur, halogen,...), thu được dẫn xuất của hydrocarbon. Dẫn xuất của hydrocarbon được phân thành nhiều loại:
a. Khái niệm
Nhóm chức là nguyên tử hoặc nhóm nguyên tử trong phân tử gây ra những tính chất hoá học đặc trưng của hợp chất hữu cơ.
Ví dụ: Dimethyl ether (H3C-O-CH3) và ethanol (C2H5-OH) có cùng công thức phân tử C2H6O nhưng có các tính chất khác nhau. Dimethyl ether không phản ứng với sodium, trong khi ethanol phản ứng với sodium giải phóng hydrogen.
2C2H5OH + 2Na → 2C2H5ONa + H2
- Nhóm -OH đã gây ra các phản ứng đặc trưng, phân biệt ethanol với dimethyl ether và với các loại hợp chất khác nên nhóm -OH được gọi là nhóm chức alcohol.
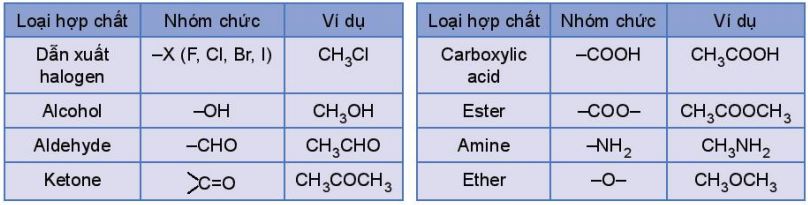
b. Một số loại nhóm chức cơ bản
Bảng 10.1. Một số nhóm chức cơ bản và công thức cấu tạo
c. Phổ hồng ngoại và nhóm chức
Phương pháp phổ hồng ngoại (Infrared Spectroscopy, được viết tắt là IR) là phương pháp vật lí rất quan trọng và phổ biến đề nghiên cứu cấu tạo phân tử hợp chất hữu cơ.
- Mỗi liên kết trong phân tử hợp chất hữu cơ hấp thụ một vài bức xạ hồng ngoại đặc trưng cho liên kết đó.
- Phổ hồng ngoại của một chất được máy phổ ghi lại tự động khi cho nguồn bức xạ hồng ngoại đi qua chất nghiên cứu.
- Phổ hồng ngoại thường biểu thị sự phụ thuộc của độ truyền qua (%) của bức xạ hồng ngoại vào số sóng (cm−1).
- Các cực tiểu truyền qua (hoặc cực đại hấp thụ) ứng với dao động của các liên kết trong phân tử chất nghiên cứu được gọi là các tín hiệu (hoặc peak).
- Dựa vào các số sóng hấp thụ đặc trưng trên phổ IR có thể dự đoán nhóm chức trong phân tử chất nghiên cứu.
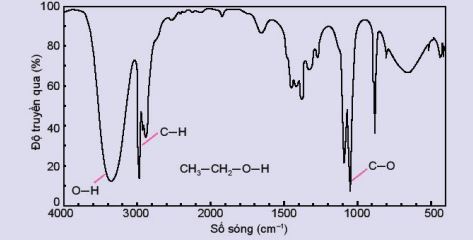
Ví dụ:
Hình 10.2. Phổ hồng ngoại của ethanol
- Bảng 10.2 là số sóng đặc trưng của một số nhóm chức cơ bản (phổ hồng ngoại).